
Con el aumento de las temperaturas en esta época del año los alimentos deben conservar la cadena de frío, ser manipulados correctamente y lavados con agua segura. Además, es necesario tener ciertos recaudos al comprar.
El Ministerio de Salud resolvió el viernes, no autorizar en territorio neuquino la venta libre de productos médicos con metodología rápida para la detección de antígenos virales de SARS-Cov-2.
Salud01/05/2021 Redacción NA
Redacción NA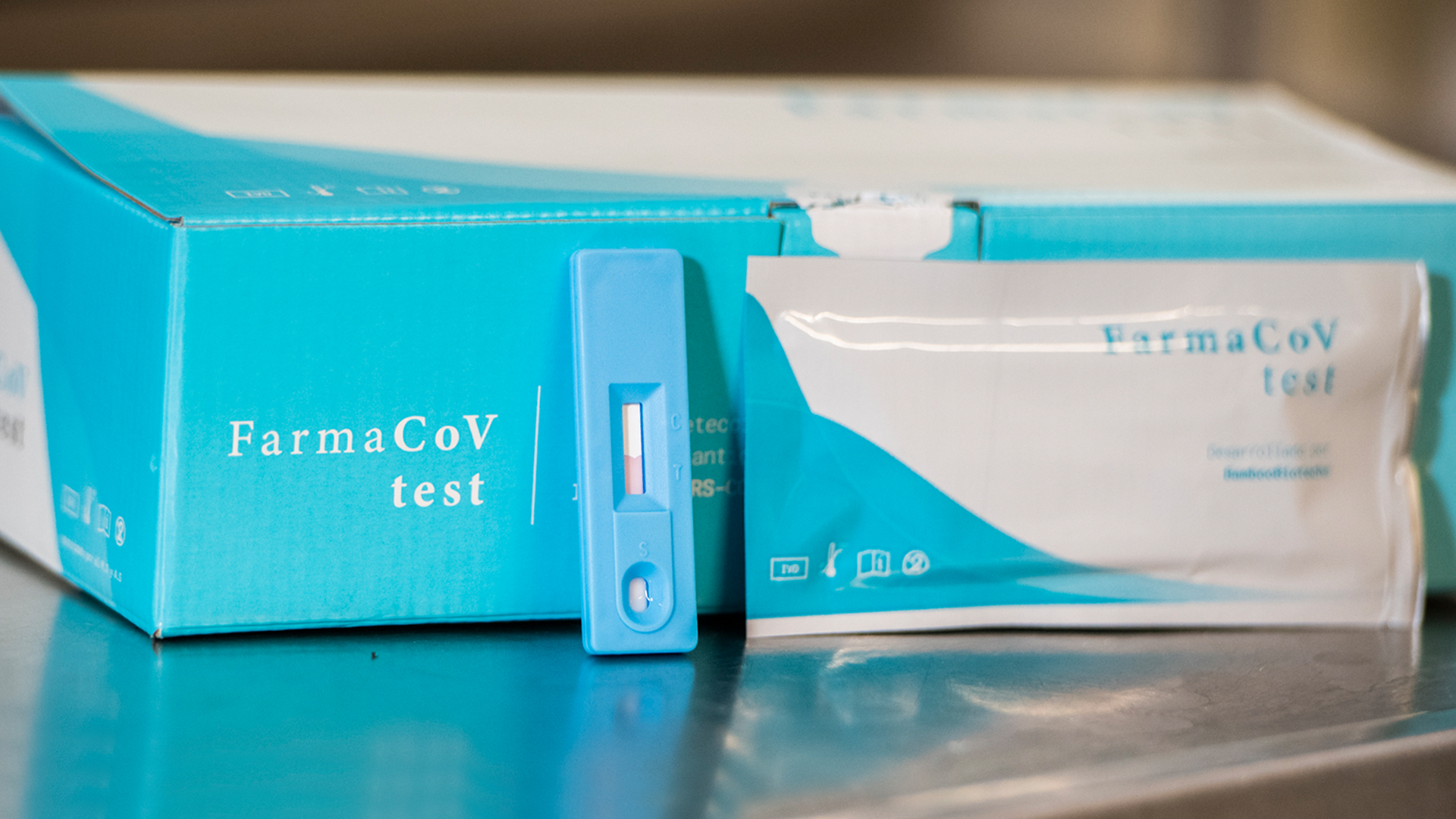
En la resolución publicada por el Ministerio de Salud además autoriza exclusivamente a las distribuidoras de productos médicos habilitadas por la Subsecretaría de Salud la compra y venta de los test rápidos.
Compartimos el texto completo de la misma.
Número:
Referencia: EX-2021-00413274- NEU-DESP#MS
VISTO:
El EX-2021-00413274- NEU-DESP#MS, del registro de la Mesa de Entradas y Salidas dependiente del
Ministerio de Salud; y
CONSIDERANDO:
Que el 11 de Marzo de 2020 la Organización Mundial de la Salud (OMS) declaró el brote de coronavirus
(COVID-19) como pandemia;
Que el Poder Ejecutivo Nacional mediante Decreto Nº 260/20 amplió la emergencia pública en materia
sanitaria establecida por Ley 27.541 por el plazo de un (1) año en virtud de la pandemia declarada;
Que a través de la Ley provincial 3230, reglamentada mediante el Decreto Nº 0414/20, se declara la
emergencia sanitaria en todo el territorio de la Provincia del Neuquén en virtud de la declaración de la
Organización Mundial de la Salud como pandemia del coronavirus (COVID-19) por el plazo de ciento
ochenta (180) días, prorrogable por igual término por única vez y se facultó al Poder Ejecutivo para que a
través del órgano de aplicación adopte una serie de medidas necesarias para atender a la emergencia
sanitaria declarada;
Que mediante el Decreto Nacional Nº 167/21 el Gobierno Nacional dispuso prorrogar la emergencia
sanitaria dispuesta mediante el Decreto Nº 260/20, hasta el día 31 de diciembre de 2021;
Que por su parte el Gobierno de la Provincia del Neuquén mediante el DECTO-2021-488-NEU-GPN
adhirió a dicha medida;
Que la serie de medidas adoptadas a nivel provincial, se han dictado con el primordial fin de contener y
mitigar la propagación de la epidemia del coronavirus (COVID-19), y con su aplicación se pretende
proteger la salud pública, adoptándose en tal sentido medidas proporcionadas a la amenaza que se enfrenta,
en forma razonable y temporaria;
Que en el marco de las acciones llevadas a cabo por el Ministerio de Salud de la Provincia de Neuquén en
relación a la detección y control del COVID-19, es importante destacar que toda metodología rápida para la
detección de antígenos virales de SARS-Cov-2, como así también anticuerpos anti SARS-Cov-2, debe ser
realizada en los establecimientos habilitados para tal fin, según lo especificado en la Resolución Nº 414/20
de este Ministerio de Salud, bajo los protocolos vigentes y con supervisión profesional, y que en el contexto del sistema de Salud Pública, se lleva a cabo con personal capacitado, con la supervisión de profesionales
bioquímicos y la correspondiente notificación epidemiológica al Sistema Nacional de Vigilancia;
Que en virtud de las autorizaciones emitidas por la Administración Nacional de Medicamentos, Alimentos,
y Tecnología Médica (ANMAT), en relación a productos con metodología rápida para la detección de
antígenos virales de SARS-Cov-2, como así también anticuerpos anti SARS-Cov-2, los mismos son de
USO PROFESIONAL EXCLUSIVO e instituciones sanitarias;
Que tal como lo ha establecido la ANMAT en su Disposición 9688/19, el “uso profesional exclusivo e
instituciones sanitarias” se corresponde con aquellos productos médicos que, debido a su riesgo intrínseco,
o en razón de su modo de uso, o a las medidas colaterales necesarias para su uso, no resultan seguros si no
son utilizados por un profesional habilitado para utilizar dicho producto de acuerdo con sus incumbencias
profesionales. Consecuentemente estos productos sólo podrán ser vendidos a instituciones sanitarias;
Que el incumplimiento del uso profesional exclusivo descripto, puede generar responsabilidades de los
actores que participen y faciliten su incumplimiento a raíz de las obligaciones profesionales
reglamentariamente establecidas, de las que son autoridad de aplicación la Subsecretaria de Salud;
Que los profesionales habilitados por sus alcances profesionales y actividades reservadas son los
profesionales Bioquímicos, para su correcta manipulación, utilización, manejo adecuado de residuos
peligrosos, informe de resultados y denuncias al Sistema Nacional de Vigilancia;
Que en la provincia de Neuquén se encuentra vigente la Resolución 935/14 de este Ministerio, en la cual en
su Artículo 1°: “ESTABLECE que la presente se aplicará a las personas físicas o jurídicas que realicen
actividades de adquisición, reprocesamiento, almacenamiento, distribución, entrega, dispensa, comercio al
por mayor y/o menor de productos médicos…”, debiendo obtener la habilitación de sus establecimientos
como Distribuidor de productos Médicos, para realizar estas actividades;
Que una prueba diagnóstica inadecuada podría pasar por alto pacientes con infección activa o categorizar
falsamente a los pacientes con la enfermedad cuando no la tienen, lo que obstaculiza los esfuerzos de
control de la enfermedad;
Que el circuito de abordaje de COVID – 19 no solo implica la detección de personas que estén cursando la
infección, sino que es fundamental el aislamiento inmediato de los casos confirmados, investigación
epidemiológica, rastreó de contactos estrechos y carga de datos al sistema Epidemiológico de Vigilancia;
Que ha tomado debida intervención la Dirección de Legal y Técnica de la Subsecretaría de Salud;
Por ello y en el uso de sus atribuciones;
LA MINISTRA DE SALUD
RESUELVE:
Artículo 1°: AUTORIZAR exclusivamente a las DISTRIBUIDORAS DE PRODUCTOS MÉDICOS
habilitadas por esta Subsecretaría de Salud, a la compra y venta de los productos médicos con metodología
rápida para la detección de antígenos virales de SARS-Cov-2, como así también anticuerpos anti SARS-
Cov-2.
Artículo 2°: AUTORIZAR la adquisición de los productos médicos con metodología rápida para la
detección de antígenos virales de SARS-Cov-2, como así también anticuerpos anti SARS-Cov-2 a las
Instituciones de Salud ya habilitadas según Resolución N° 414/20 para el diagnóstico de SARS-Cov-2
(COVID – 19).
Artículo 3º: NO AUTORIZAR la venta de los insumos médicos descriptos en el artículo 1° de la presente al público en general.
Artículo 4º: Es Obligatorio dar estricto cumplimiento por parte de los establecimientos que realizan el
diagnóstico, con la notificación epidemiológica de casos al Sistema Nacional de Vigilancia (SISA).
Artículo 5°: Serán de aplicación el régimen sancionatorio previsto en la Ley de Farmacia N° 17565 y
Decreto Reglamentario N° 2577/77.
Artículo 6°: Comuníquese, publíquese, agréguese copia a sus antecedentes y archívese.

Con el aumento de las temperaturas en esta época del año los alimentos deben conservar la cadena de frío, ser manipulados correctamente y lavados con agua segura. Además, es necesario tener ciertos recaudos al comprar.

Estas unidades permiten renovar y fortalecer la flota sanitaria para brindar mayor accesibilidad.

El viernes 19 de diciembre se realizará una jornada de vacunación extendida en toda la provincia. Es abierta a la comunidad, y estarán disponibles todas las vacunas del calendario.

Fueron 13 personas las que recibieron su certificado; apostando a la formación de calidad y el desarrollo de competencias claves en el ámbito de la salud y la alimentación segura.

Desde la cartera sanitaria aconsejan mantener la higiene en la vivienda y los alrededores, así como colocar mosquiteros y burletes en las aberturas y no intentar capturarlos.
Se trata de una enfermedad infecciosa altamente contagiosa que afecta las vías respiratorias y puede ser grave en bebés menores de 6 meses. Hubo siete casos de muerte en el país por esa causa.

Una joven de 30 años oriunda de Buenos Aires sufrió una caída en la zona de alta montaña y fue asistida por rescatistas del Parque Nacional Lanin. El operativo, que incluyó dos cuadrillas y coordinación con el Hospital de Junín de los Andes, culminó con éxito en horas de la tarde.

El Ministerio Público Fiscal (MPF) y la Policía provincial realizaron cuatro allanamientos en el contexto de la investigación iniciada por la presunta adulteración de cocaína, que fue comercializada a personas consumidoras en la ciudad de Neuquén.

Rolando Alberto Labrousse reemplaza como comandante al coronel mayor Pablo Conforte, quien se despidió del servicio activo.

Las capacitaciones tuvieron como objetivo fortalecer habilidades laborales y acompañar la inserción de neuquinos y neuquinas en el mercado de trabajo.

La remodelación y ampliación de la terminal consolidará la conectividad aérea y acompañará el crecimiento sostenido del turismo en la región de los Lagos del Sur. Además, mejorará la experiencia de los usuarios y potenciará el perfil internacional de los destinos neuquinos.